Sau khi ghi nhận ca nhiễm Covid-19 đầu tiên ở Việt Nam vào ngày 23.1.2020, Bộ KH-CN đã phê duyệt đề tài nghiên cứu được thực hiện giữa Học viện Quân y và Công ty CP Công nghệ Việt Á (VietACorp).
Ngày 2.3.2020, Bộ trưởng Bộ KH-CN ban hành Quyết định số 489/QĐ-BKHCN thông qua kết quả đề tài “Nghiên cứu chế tạo bộ sinh phẩm RT-PCR và realtime RT-PCR phát hiện chủng virus corona mới 2019 (2019-nCoV)”.
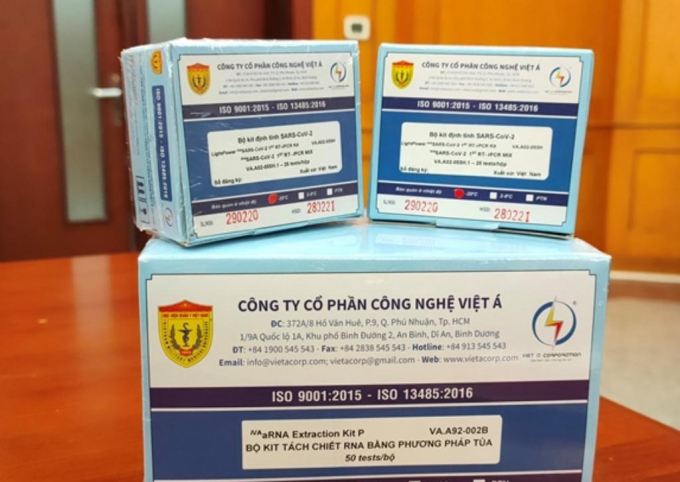
Ngày 3.3.2020, Hội đồng đánh giá, nghiệm thu kết quả giai đoạn 1 đề tài này đã họp và đề nghị Bộ Y tế cấp phép sử dụng cho 2 bộ sinh phẩm realtime PCR chẩn đoán SARS-CoV-2 (LightPoweriVA SARS-CoV-2 1st RT-PCR Kit, LightPoweriVA SARS-CoV-2 1st RT-rPCR Kit). Chỉ sau đó 1 ngày, tức này 4.3.2020, Bộ Y tế đồng ý cấp phép cho kit test của VietACorp và Học viện Quân y.
 |
Bộ Y tế cho biết khi cấp phép đã căn cứ vào ý kiến của hội đồng và căn cứ vào kết quả đánh giá đáp ứng về độ nhạy và độ đặc hiệu của Viện Vệ sinh dịch tễ T.Ư.
Ngoài ra, còn có kết quả xác nhận cơ sở sản xuất của công ty đã đạt tiêu chuẩn ISO 13485:2016 do Tổ chức Bureau Veritas cấp (đây là tổ chức đã được Bộ KH-CN công nhận) và theo các quy định tại Nghị định 36/2016/NĐ-CP, Nghị định 169/2018/NĐ-CP, Bộ Y tế đã cấp phép sử dụng tạm thời cho 2 bộ sinh phẩm nói trên trong thời hạn 6 tháng, từ ngày 4.3.2020, để sử dụng trong xét nghiệm sàng lọc. Về việc này, Bộ Y tế cho biết đã đảm bảo đáp ứng nhu cầu xét nghiệm tại thời điểm rất khó khăn khi tiếp cận với nguồn cung ứng sinh phẩm trên thế giới.
Dến ngày 4.12.2020, Bộ này đã có Quyết định số 5071/QĐ-BYT cấp phép lưu hành 5 năm đối với bộ sinh phẩm xét nghiệm SARS-CoV-2 chủng loại LightPoweriVA SARS-CoV-2 1st RT-rPCR Kit của Công ty CP Công nghệ Việt Á.
Bộ Y tế cấp phép lưu hành cho sinh phẩm xét nghiệm SARS-CoV-2 chủng loại One-Step RT- PCR COVID-19 Kit Thai Duong Multiplex-3 target genes Version 1.0 của Công ty CP Sao Thái Dương.
Tính đến ngày 20.12.2021, Bộ Y tế cho biết đã cấp phép 146 sinh phẩm xét nghiệm SARS-CoV-2, trong đó có 46 sinh phẩm xét nghiệm vật liệu di truyền (PCR, LAMP) tương tự như sản phẩm của VietACorp và Công ty CP Sao Thái Dương (bao gồm 7 sinh phẩm sản xuất trong nước và 39 sinh phẩm nhập khẩu).
Bộ Y tế xác định việc cấp phép cho nhiều sản phẩm là để tăng cường nội địa hóa, chủ động nguồn cung và tạo sự cạnh tranh về giá sinh phẩm xét nghiệm. Tất cả các sản phẩm cấp phép đều đã được đánh giá đạt yêu cầu, đáp ứng tiêu chuẩn, chất lượng của Việt Nam và đảm bảo đúng theo các quy định hiện hành.
Bộ Y tế cho rằng, danh mục các sinh phẩm do WHO công bố và đưa vào danh sách sử dụng khẩn cấp (EUL), các công ty mong muốn sản phẩm của mình được đưa vào danh sách của WHO thì nộp hồ sơ đề nghị WHO xem xét.
Theo Bộ Y tế, mỗi quốc gia, tổ chức đều xây dựng tiêu chí và yêu cầu về hồ sơ, sản phẩm khác nhau về việc chấp thuận lưu hành sinh phẩm. Các công ty có nhu cầu lưu hành, sử dụng tại quốc gia và tổ chức nào sẽ nộp hồ sơ theo quy định của từng tổ chức, quốc gia đó.
“Do vậy, việc cấp phép của Bộ Y tế đối với sản phẩm của Công ty CP Công nghệ Việt Á và các nhà sản xuất khác không phụ thuộc vào danh sách do WHO công bố. Tính đến nay, đối với sinh phẩm xét nghiệm PCR, theo danh sách EUL của WHO có 23 sản phẩm được phê duyệt; trong khi đó, tại châu Âu đã chấp thuận 589 loại sinh phẩm, Mỹ chấp thuận sử dụng 276 loại sinh phẩm, Hàn Quốc chấp thuận sử dụng trong nước 31 sinh phẩm...”, Bộ Y tế lý giải.